发布时间:2024-01-16 来源:Med-techNews; MHRA 作者:

英国药品和保健产品监管局(Medicines & Healthcare products Regulatory Agency,MHRA)制定英国医疗器械新法规的新计划。新法规将把患者安全放在第一位,并有助于确保患者继续立即获得所需的医疗器械,同时增强英国作为世界领先的医疗技术创新环境的地位。
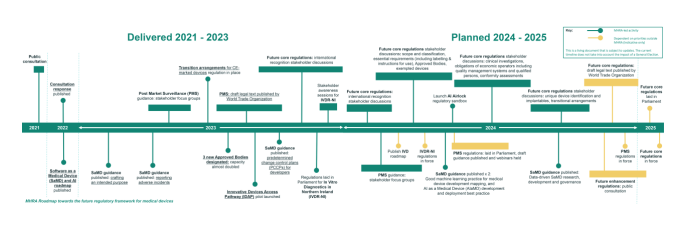
MHRA新法规的“路线图”旨在增强英国从快速发展的医疗技术中受益的能力,为患者和医疗保健提供新的机会。路线图制定了通过一系列新的法定工具(Statutory Instruments,SI)提供有利监管的路线。今年将实施保护患者安全的优先措施,新框架的核心要素预计到2025年落实到位。计划中的法规还旨在实现更大程度的国际协调,对响应技术进步的医疗器械提出更加以患者为中心并相称的要求。
MHRA医疗技术监管改革负责人兼医疗保健、质量和可及性首席官员Laura Squire博士表示:“当今令人兴奋的医疗技术进步为患者护理和改善医疗服务提供了重要的新机遇。因此,我们很高兴在新的一年开始之际制定一项全面计划,并在未来两年内显着改进医疗器械的监管框架。新框架将增强MHRA保护患者安全的能力,同时营造一个鼓励推出最具创新性的医疗保健产品的环境,这些产品对公众的健康产生真正的影响。该路线图阐明了随着进程的推进,我们将如何与包括患者在内的利益相关者合作,尽早了解即将发生的事情,并向我们提供有关他们所需指导的反馈,以确保成功实施这些广泛的改革。”
英国健康科技产业协会(Association of British HealthTech Industries,ABHI)首席执行官Peter Ellingworth补充:“国际认可将确保英国患者能够持续获得安全有效的健康技术,这既可以增强生命,又可以挽救生命。今天的路线图公布是向着这方面迈出的重要一步,有助于推动英国的创新和增长,同时使本土企业能够扩大其全球影响力。我们期待与MHRA合作,并通过国际医疗器械监管机构论坛(International Medical Device Regulators Forum,IMDRF)和全球医疗技术联盟(GMTA,Global Medical Technology Alliance)等国际论坛保持参与,以确保成功实施。”
英国体外诊断协会(British in vitro Diagnostics Association,BIVDA)临时首席执行官Helen Dent评论:“BIVDA欢迎MHRA为英国新医疗器械法规制定路线图的做法。患者安全和可及性至关重要,草拟的时间表反映了我们朝着实现这些目标迈出的积极一步。我们期待继续与MHRA、行业利益相关者和我们的成员密切合作,以确保这些法规的成功实施。”
Source: Med-techNews; MHRA





